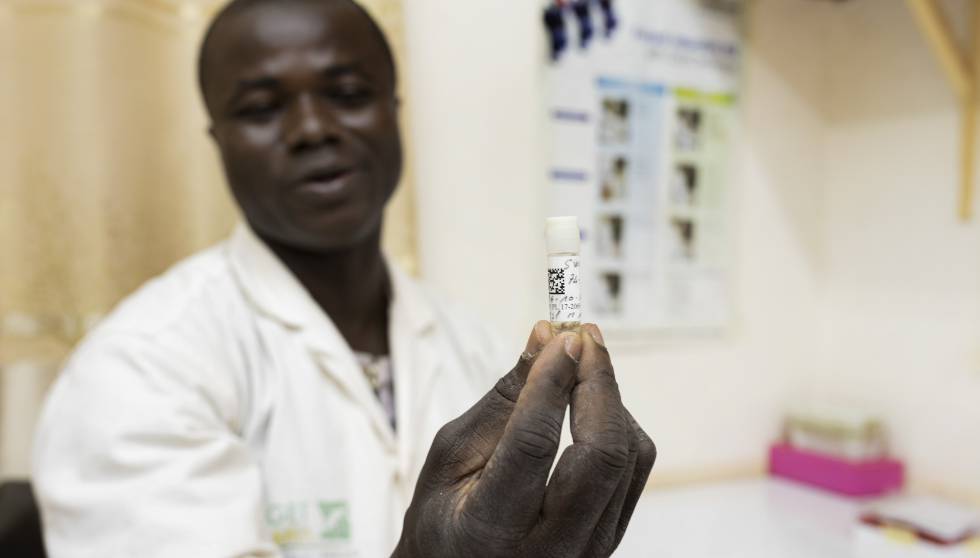
En el ala derecha de un vetusto edificio amarillo de las afueras de Bobo-Dioulasso, en Burkina Faso, el entomólogo Moussa Namountougou abre con extremo cuidado una puerta.
De un solo paso accede al insectario. Miles de mosquitos son criados por una nueva hornada de científicos burkineses; esto a una temperatura estable de 28 grados centígrados.
“Hemos tomado todas las precauciones para que no se produzca ninguna fuga”, asegura Namountougou, “estas instalaciones tienen el nivel óptimo para el confinamiento de artrópodos, avalado por la Agencia Nacional de Bioseguridad”, explica.
Mosquiteras, climatización, puertas dobles y trampas: la seguridad es una auténtica obsesión.
La malaria
La malaria no es una cuestión baladí. Según la Organización Mundial de la Salud (OMS), solo en 2017 afectó a 219 millones de personas y provocó 435.000 muertes, de las que un 90% se produjeron en África, sobre todo niños menores de cinco años.
El parásito se transmite al ser humano a través de la picadura de la hembra de varias especies de mosquitos del género Anopheles, que necesita la sangre para madurar los huevos que lleva en su interior una vez ha sido fecundada.
El ser humano lleva siglos luchando contra este pequeño gran enemigo con medicamentos, pulverizadores, repelentes, mosquiteras impregnadas de insecticida y, desde hace tan solo unos meses, con una vacuna desarrollada en Mozambique con un importante apoyo español.
Existen 3.500 especies de mosquitos en el mundo y 840 en África, de las que tan solo cuatro transmiten el parásito del paludismo
Sin embargo, sigue matando a gran escala. Target Malaria, un consorcio internacional no lucrativo impulsado por la Fundación Bill y Melinda Gates y el Open Philanthropy Project Fund y apoyado por 13 instituciones públicas y privadas del mundo, surge como alternativa a esos métodos.
“Los mosquitos son cada vez más resistentes a las moléculas con las que tratamos de eliminarlos y la vacuna tiene una eficacia limitada, sobre todo en los niños de pecho, que es el tramo de edad más peligroso”, asegura el entomólogo médico Abdoulaye Diabaté, investigador principal del proyecto en Burkina Faso.
“Es unánime la opinión de que solo con mosquiteras y con la actual vacuna no podremos acabar con la enfermedad”.
Troyano informático
En la sala de Biología Molecular del insectario del Instituto de Investigación en Ciencias de la Salud (IRSS), en Bobo Dioulasso, el científico Dao Koulmaga extrae y amplifica el ADN de un mosquito.
Estas instalaciones se crearon en 2014. “Dos años más tarde y con todos los permisos necesarios recibimos los primeros 500 huevos modificados genéticamente”, asegura el doctor Namountougou.
La idea surgió en el Imperial College de Londres, una de las universidades más prestigiosas del mundo. Consiste en implantar en el animal un gen defectuoso que reduzca de manera significativa la población de la especie. A la vez que se transmita de una generación a otra, como si se tratara de un troyano informático. ¿Cómo hacerlo? Manipulando las leyes de la herencia. A esta tecnología se la denomina Gene Drive o impulso genético.
La modificación que afectaba a los 500 huevos importados en 2016 provocaba que los machos nacieran estériles; mientras las hembras no, aunque sí tenían la capacidad de transmitir el gen alterado a su descendencia.
Liberan 6.400 ejemplares de machos estériles
Desde entonces han pasado más de 40 generaciones de mosquitos criados, observados, alimentados y cruzados con esmero en el insectario. El pasado 1 de julio, Target Malaria libero 6.400 ejemplares de machos estériles. Estos murieron en unos días sin dejar descendencia en la localidad de Bana, cercana a Bobo-Dioulasso.
Los insectos copulan con la hembra, pero los huevos que esta produce no eclosionan. Esto es porque el gen modificado acaba por desaparecer. Además, el mosquito macho no pica al ser humano porque no necesita la sangre.
“Fue solo una prueba. La idea era recoger el máximo de datos posible respecto a su dispersión en la naturaleza; igualmente, el tiempo de supervivencia y comportamiento, si por ejemplo se agrupan en nubes. Y cómo se mezclan con los ejemplares salvajes locales”, explica Diabaté.
El experimento apenas tendrá impacto sobre la incidencia de la malaria en la zona.